giovedì 31 luglio 2008
venerdì 25 luglio 2008
Marea ti voglio!
Che estate sarebbe senza Lapo(lverina) Elkann?
Tre sere fa, pare che il creatore di personal belongings, di mondi nuovi, mondi che uniscono il vecchio con il nuovo - "ah, tutto questo so' 'ji occhiali?" (Enrico Lucci) - si sia dato alla rivendicazione di taxi altrui: una Marea, di sua proprietà in quanto Fiat.
 Ora, mio caro Lapo: sei stato fortunato che la notte brava l'hai fatta a Capri. Perché se hai intenzione di replicarla dalle mie parti - va be', al massimo potrai farti il giro delle osterie - sappi che anche io guido una Marea (non decappottabile!). E non so se sarei gentile come Pietro Vanacore.
Ora, mio caro Lapo: sei stato fortunato che la notte brava l'hai fatta a Capri. Perché se hai intenzione di replicarla dalle mie parti - va be', al massimo potrai farti il giro delle osterie - sappi che anche io guido una Marea (non decappottabile!). E non so se sarei gentile come Pietro Vanacore.
Canzone del giorno: The Cure - Just Like Heaven.
Tre sere fa, pare che il creatore di personal belongings, di mondi nuovi, mondi che uniscono il vecchio con il nuovo - "ah, tutto questo so' 'ji occhiali?" (Enrico Lucci) - si sia dato alla rivendicazione di taxi altrui: una Marea, di sua proprietà in quanto Fiat.
 Ora, mio caro Lapo: sei stato fortunato che la notte brava l'hai fatta a Capri. Perché se hai intenzione di replicarla dalle mie parti - va be', al massimo potrai farti il giro delle osterie - sappi che anche io guido una Marea (non decappottabile!). E non so se sarei gentile come Pietro Vanacore.
Ora, mio caro Lapo: sei stato fortunato che la notte brava l'hai fatta a Capri. Perché se hai intenzione di replicarla dalle mie parti - va be', al massimo potrai farti il giro delle osterie - sappi che anche io guido una Marea (non decappottabile!). E non so se sarei gentile come Pietro Vanacore.Canzone del giorno: The Cure - Just Like Heaven.
martedì 22 luglio 2008
vi
Devo ammettere che, dopo una certa iniziale diffidenza, nonostante alla mia postazione usi ancora Emacs, sto cominciando ad apprezzare l'editor di testi vi. Sarà perché i suoi comandi da tastiera mi ricordano il mitico WordStar?
Canzone del giorno: Katatonia - Day.
Canzone del giorno: Katatonia - Day.
lunedì 21 luglio 2008
Forse, forse...
... ci siamo!
Sto simulando argon a temperatura 1,40 e densità 0,681641.
Stando ai dati di riferimento, dovrei ottenere una pressione di 1,09541.
(Le quantità sono espresse in unità ridotte.)
Ho ottenuto 1,18291. Con una deviazione standard di 0,20529. E il tempo di simulazione era piuttosto breve.
Che dite, sono sulla buona strada?
Canzone del giorno: The Strokes - Soma.
Sto simulando argon a temperatura 1,40 e densità 0,681641.
Stando ai dati di riferimento, dovrei ottenere una pressione di 1,09541.
(Le quantità sono espresse in unità ridotte.)
Ho ottenuto 1,18291. Con una deviazione standard di 0,20529. E il tempo di simulazione era piuttosto breve.
Che dite, sono sulla buona strada?
Canzone del giorno: The Strokes - Soma.
domenica 20 luglio 2008
Piazza Navona (2) - Marco Travaglio
Dicevo che Marco Travaglio, pur leggendo sempre volentieri i suoi articoli, ultimamente mi sta piacendo assai meno.
In parte perché - l'ho notato in prima persona, nel ricevere risposta a una domanda alla presentazione di Inciucio - mi pare molto pieno di sé: come dire, uno che sa di essere preparato e che lo fa pesare sugli altri. Ciò lo porta anche a dispensare "patenti di giornalista libero" : per esempio al V2-Day, il 25 aprile scorso, disse che al Corriere c'è tanta spazzatura, ma "c'è anche Gian Antonio Stella, c'è Sergio Rizzo..." - ottimi giornalisti, ma guarda caso, proprio i due autori della Casta, una delle Bibbie dei grillini. Un giornalista che si propone come giudice dei suoi colleghi, onestamente, mi sta un po' sulle palle.
Forse esagero, ma credo che gli abbia fatto male la vicinanza a Beppe Grillo. Anzitutto, perché un giornalista dovrebbe essere il primo a rimarcare l'importanza di attingere da più fonti, ed è l'esatto opposto di Grillo, il cui motto è: io dico la verità, e chi mi critica è al soldo di mafie. So che probabilmente questo, più che il suo, è il motto dei suoi fans, ma non è che lui faccia molto per smentirlo: pensiamo agli insulti, comparsi sul suo blog, a Gianni Riotta - ancor prima che costui fosse nominato al vertice del Tg1 - colpevole di averlo contestato su una questione scientifica.
Ora Travaglio sbandiera un 29,4% di favorevoli al No Cav Day, nonostante la mistificazione dei media. Ma dimentica che non sta parlando di una quota di mercato: sta parlando di votanti, e di fronte ad un 55% di contrari (la fonte è la stessa: un sondaggio di Renato Mannheimer) quel 29,4% si scioglie come burro al sole. Anzi, considerato quanto partigiana è l'Italia, il 29,4% è una percentuale infima.
Già all'indomani del primo V-Day (8 settembre 2007), secondo Travaglio, quei 336 mila che avevano sottoscritto le proposte di Grillo - limite dei due mandati per i parlamentari, ineleggibilità per i condannati in via definitiva, reintroduzione delle preferenze - erano una cifra stratosferica: la Casta sarebbe stata travolta. Si è visto: poco più di un mese dopo, un numero di cittadini dieci volte superiore andò a votare - pagando pure! - alle primarie del Partito Democratico.
Travaglio si ostina a dileggiare chi afferma che agli italiani il conflitto d'interessi, il duopolio Rai-Mediaset, le leggi ad personam... importino poco; peccato che le cose stiano proprio così.
Ha tanto detto della Rosa nel Pugno, il partito che "piace alla gente che piace" come la Y10, ma che alle elezioni non va oltre un misero 2,5%. E non si accorge che l'Italia dei Valori - altra cosa: Travaglio si era sempre dichiarato un cane sciolto, non facente parte di alcuna destra o sinistra organizzata; lo dico con dispiacere, ma dopo tutte le manifestazioni con Di Pietro non è più credibile in tal senso - manifesta gli stessi difetti.
Mi immagino la conversazione, ad un gazebo, tra un militante dipietrista e un potenziale elettore. Il dipietrista, infervorato: "l'Italia deve essere un Paese dove la legge sia uguale per tutti, dove la magistratura possa indagare senza politici che si intromettano; noi dell'Italia dei Valori ci batteremo per un Paese giusto!" Il potenziale elettore, distratto: "va bene, va bene... ma quanto si paga?"
Non so se il mio celebre omonimo leggerà mai le mie parole: in tal caso, si ricordi che gli voglio bene e che continuerò a leggerlo; ma che per tutti arriva l'età in cui gli idoli vanno de-idolatrati! :-)
Canzone del giorno: Franz Ferdinand - Evil And A Heathen.
In parte perché - l'ho notato in prima persona, nel ricevere risposta a una domanda alla presentazione di Inciucio - mi pare molto pieno di sé: come dire, uno che sa di essere preparato e che lo fa pesare sugli altri. Ciò lo porta anche a dispensare "patenti di giornalista libero" : per esempio al V2-Day, il 25 aprile scorso, disse che al Corriere c'è tanta spazzatura, ma "c'è anche Gian Antonio Stella, c'è Sergio Rizzo..." - ottimi giornalisti, ma guarda caso, proprio i due autori della Casta, una delle Bibbie dei grillini. Un giornalista che si propone come giudice dei suoi colleghi, onestamente, mi sta un po' sulle palle.
Forse esagero, ma credo che gli abbia fatto male la vicinanza a Beppe Grillo. Anzitutto, perché un giornalista dovrebbe essere il primo a rimarcare l'importanza di attingere da più fonti, ed è l'esatto opposto di Grillo, il cui motto è: io dico la verità, e chi mi critica è al soldo di mafie. So che probabilmente questo, più che il suo, è il motto dei suoi fans, ma non è che lui faccia molto per smentirlo: pensiamo agli insulti, comparsi sul suo blog, a Gianni Riotta - ancor prima che costui fosse nominato al vertice del Tg1 - colpevole di averlo contestato su una questione scientifica.
Ora Travaglio sbandiera un 29,4% di favorevoli al No Cav Day, nonostante la mistificazione dei media. Ma dimentica che non sta parlando di una quota di mercato: sta parlando di votanti, e di fronte ad un 55% di contrari (la fonte è la stessa: un sondaggio di Renato Mannheimer) quel 29,4% si scioglie come burro al sole. Anzi, considerato quanto partigiana è l'Italia, il 29,4% è una percentuale infima.
Già all'indomani del primo V-Day (8 settembre 2007), secondo Travaglio, quei 336 mila che avevano sottoscritto le proposte di Grillo - limite dei due mandati per i parlamentari, ineleggibilità per i condannati in via definitiva, reintroduzione delle preferenze - erano una cifra stratosferica: la Casta sarebbe stata travolta. Si è visto: poco più di un mese dopo, un numero di cittadini dieci volte superiore andò a votare - pagando pure! - alle primarie del Partito Democratico.
Travaglio si ostina a dileggiare chi afferma che agli italiani il conflitto d'interessi, il duopolio Rai-Mediaset, le leggi ad personam... importino poco; peccato che le cose stiano proprio così.
Ha tanto detto della Rosa nel Pugno, il partito che "piace alla gente che piace" come la Y10, ma che alle elezioni non va oltre un misero 2,5%. E non si accorge che l'Italia dei Valori - altra cosa: Travaglio si era sempre dichiarato un cane sciolto, non facente parte di alcuna destra o sinistra organizzata; lo dico con dispiacere, ma dopo tutte le manifestazioni con Di Pietro non è più credibile in tal senso - manifesta gli stessi difetti.
Mi immagino la conversazione, ad un gazebo, tra un militante dipietrista e un potenziale elettore. Il dipietrista, infervorato: "l'Italia deve essere un Paese dove la legge sia uguale per tutti, dove la magistratura possa indagare senza politici che si intromettano; noi dell'Italia dei Valori ci batteremo per un Paese giusto!" Il potenziale elettore, distratto: "va bene, va bene... ma quanto si paga?"
Non so se il mio celebre omonimo leggerà mai le mie parole: in tal caso, si ricordi che gli voglio bene e che continuerò a leggerlo; ma che per tutti arriva l'età in cui gli idoli vanno de-idolatrati! :-)
Canzone del giorno: Franz Ferdinand - Evil And A Heathen.
sabato 19 luglio 2008
Entropia per principianti (2a)
Poiché l'argomento è un po' lungo, ho deciso di dividere la seconda puntata in due semi-puntate :-)
2a. Le trasformazioni reversibili
Il concetto di trasformazione reversibile è centrale nella definizione di entropia. Vediamolo per bene, con tre esempi:
Nel primo caso: posso riportare il libro in moto? Certamente, se lo spingo. Nel secondo caso: posso riformare i cubetti di ghiaccio? Certamente, se uso un freezer. Nel terzo caso: posso riportare il gas tutto nel primo serbatoio? Certamente, se uso una pompa.
Dov'è il trucco? In tutti e tre i casi, devo compiere lavoro dall'esterno: l'esterno (ambiente), di conseguenza, resta irreversibilmente modificato.
Ai confini della realtà, esiste un caso limite: le trasformazioni reversibili.
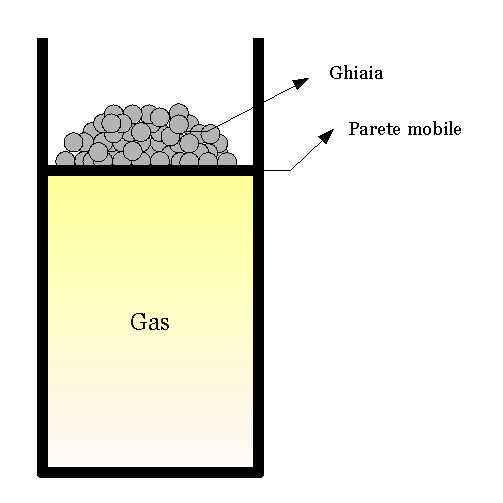 Supponiamo che lo stesso gas dell'esempio 3 sia contenuto in un recipiente con la parete superiore mobile - pensiamo al cilindro di un motore - che può scorrere senza attrito.
Supponiamo che lo stesso gas dell'esempio 3 sia contenuto in un recipiente con la parete superiore mobile - pensiamo al cilindro di un motore - che può scorrere senza attrito.
Supponiamo anche di versare della finissima ghiaia sopra questa parete mobile, affinché il suo peso porti la pressione del gas allo stesso valore che aveva, inizialmente, nell'esempio 3.
Uno alla volta, togliamo un sassolino da sopra la parete mobile: ciò riduce la pressione e fa espandere il gas.
Proseguiamo così finché il volume del gas è raddoppiato (e la pressione dimezzata), come nello stato finale dell'esempio 3.
Qual è la differenza con l'esempio 3?
Qui la trasformazione avviene molto lentamente: negli stati intermedi c'è sempre equilibrio, e non ci sono forze dissipative (attriti). Al contrario, prima la trasformazione era rapida, e gli stati intermedi (mentre il gas si espandeva) non erano affatto di equilibrio.
Variando di pochissimo le condizioni esterne - nell'esempio: aggiungendo i sassolini, anziché togliendoli - posso invertire il verso della trasformazione, e tornare alla situazione iniziale senza aver modificato l'ambiente!
Se il sistema, con la trasformazione (reversibile) diretta, assorbe il calore Q, con quella inversa ne cederà una quantità identica; e se il sistema, con la trasformazione diretta, compie il lavoro W, con quella inversa ne subirà una quantità identica.
Questa è chiaramente una circostanza irrealizzabile: gli attriti non si possono eliminare del tutto, e per quanto i sassolini siano piccoli, tra la rimozione di un sassolino e il disporsi del gas al nuovo equilibrio ci sono sempre degli stati di non equilibrio.
Lo consideriamo un caso ideale, limite delle situazioni reali.
Gli attriti, si sa, sviluppano calore - calore che potrebbe essere trasformato in lavoro - pertanto è facile intuire che il rendimento di una macchina che opera con trasformazioni irreversibili (di seguito: macchina irreversibile) sarà minore di quello di una macchina reversibile.
Nella prossima semi-puntata, vedremo qual è la macchina (ideale) che ha il rendimento più alto di tutte. E saremo pronti, finalmente, per scoprire cos'è l'entropia!
Canzone del giorno: Baustelle - Colombo.
2a. Le trasformazioni reversibili
Il concetto di trasformazione reversibile è centrale nella definizione di entropia. Vediamolo per bene, con tre esempi:
- il sistema sia un tavolo con un libro che ci scivola sopra. A un certo punto, l'attrito fermerà il libro.
L'energia totale, come è noto, si conserva: si può notare un aumento della temperatura. Cioè, l'energia cinetica iniziale del libro si è trasformata in energia termica.
Tuttavia, il viceversa non accade mai: per quanto io possa scaldare un libro fermo, esso non si metterà mai in moto; - il sistema sia un bicchiere d'acqua a temperatura ambiente con un paio di cubetti di ghiaccio. A un certo punto il ghiaccio si sarà sciolto: il calore assorbito dai cubetti di ghiaccio sarà uguale al calore ceduto dall'acqua iniziale... e berremo più volentieri dal bicchiere. Ma nessuno di noi ha mai visto acqua fredda trasformarsi spontaneamente in ghiaccio e acqua calda, nevvero?
- il sistema sia una coppia di serbatoi identici, uniti da una valvola. Se il primo serbatoio contiene gas e il secondo è vuoto, aprendo la valvola il gas si diffonde rapidamente nel secondo serbatoio.
Anche in questo caso, spontaneamente il gas non tornerà mai tutto nel primo serbatoio.
Nel primo caso: posso riportare il libro in moto? Certamente, se lo spingo. Nel secondo caso: posso riformare i cubetti di ghiaccio? Certamente, se uso un freezer. Nel terzo caso: posso riportare il gas tutto nel primo serbatoio? Certamente, se uso una pompa.
Dov'è il trucco? In tutti e tre i casi, devo compiere lavoro dall'esterno: l'esterno (ambiente), di conseguenza, resta irreversibilmente modificato.
Ai confini della realtà, esiste un caso limite: le trasformazioni reversibili.
 Supponiamo che lo stesso gas dell'esempio 3 sia contenuto in un recipiente con la parete superiore mobile - pensiamo al cilindro di un motore - che può scorrere senza attrito.
Supponiamo che lo stesso gas dell'esempio 3 sia contenuto in un recipiente con la parete superiore mobile - pensiamo al cilindro di un motore - che può scorrere senza attrito.Supponiamo anche di versare della finissima ghiaia sopra questa parete mobile, affinché il suo peso porti la pressione del gas allo stesso valore che aveva, inizialmente, nell'esempio 3.
Uno alla volta, togliamo un sassolino da sopra la parete mobile: ciò riduce la pressione e fa espandere il gas.
Proseguiamo così finché il volume del gas è raddoppiato (e la pressione dimezzata), come nello stato finale dell'esempio 3.
Qual è la differenza con l'esempio 3?
Qui la trasformazione avviene molto lentamente: negli stati intermedi c'è sempre equilibrio, e non ci sono forze dissipative (attriti). Al contrario, prima la trasformazione era rapida, e gli stati intermedi (mentre il gas si espandeva) non erano affatto di equilibrio.
Variando di pochissimo le condizioni esterne - nell'esempio: aggiungendo i sassolini, anziché togliendoli - posso invertire il verso della trasformazione, e tornare alla situazione iniziale senza aver modificato l'ambiente!
Se il sistema, con la trasformazione (reversibile) diretta, assorbe il calore Q, con quella inversa ne cederà una quantità identica; e se il sistema, con la trasformazione diretta, compie il lavoro W, con quella inversa ne subirà una quantità identica.
Questa è chiaramente una circostanza irrealizzabile: gli attriti non si possono eliminare del tutto, e per quanto i sassolini siano piccoli, tra la rimozione di un sassolino e il disporsi del gas al nuovo equilibrio ci sono sempre degli stati di non equilibrio.
Lo consideriamo un caso ideale, limite delle situazioni reali.
Gli attriti, si sa, sviluppano calore - calore che potrebbe essere trasformato in lavoro - pertanto è facile intuire che il rendimento di una macchina che opera con trasformazioni irreversibili (di seguito: macchina irreversibile) sarà minore di quello di una macchina reversibile.
Nella prossima semi-puntata, vedremo qual è la macchina (ideale) che ha il rendimento più alto di tutte. E saremo pronti, finalmente, per scoprire cos'è l'entropia!
Canzone del giorno: Baustelle - Colombo.
mercoledì 16 luglio 2008
Apprendistato tesistico
La fase di apprendistato, si sa, non è mai troppo piacevole.
Queste settimane sono per me il periodo di apprendistato per la tesi, principalmente perché devo prendere confidenza con due cose: la meccanica statistica, della quale non so più di quanto abbia studiato per l'esame di Struttura della materia; e la programmazione, della quale, se non fosse stato per quel primo anno frequentato a Ingegneria, sarei completamente a digiuno.
Avevo già avuto modo di sfruttare il corso di Fondamenti di informatica nello scrivere le relazioni per il laboratorio di spettroscopia: i dati dell'ultimo esperimento (curva di Bragg) consistevano in 2800 file di testo; il professore ci aveva fornito due programmini per la loro analisi, ma sul mio pc non giravano, così rispolverai il manuale di Java e scrissi tutto ex novo. (Non era nulla di trascendentale: la parte più difficile fu imparare come far leggere al programma l'input da un file; il resto erano semplici operazioni sugli array.)
Ora però è Fortran (Fortran 90 per essere esatti) che devo imparare: per fortuna, essendo "roba vecchia" , non è stato troppo difficile trovare in biblioteca un manuale disponibile per il prestito.
Come benchmark, il relatore mi ha assegnato da simulare un fluido (argon) le cui particelle siano soggette a un potenziale di Lennard-Jones (forze di Van der Waals).
Potrei lavorare anche a casa, ma è meglio che stia in facoltà, visto che, se qualcosa non mi torna - evento assai frequente! - posso chiedere a un altro tesista, o al relatore stesso, o a un altro professore del gruppo - uno in particolare è da me ufficialmente adorato dopo che mi ha fatto capire i potenziali termodinamici (e le trasformazioni di Legendre) in meno di dieci minuti!
Ieri e oggi, dalla mia postazione - in una sorta di atrio, attrezzato con tre terminali - potevo sentire proprio uno di questi professori che interrogava degli studenti su fisica dello stato solido - l'esame che mi ha indirizzato verso questa tesi. L'andamento del calore specifico con la temperatura: i fononi, il modello di Debye, che si riduce alla legge di Dulong-Petit ad alte temperature... Non sono sadico, però che goduria avere finito e sapere che a stare sotto i riflettori ora tocca agli altri!
Canzone del giorno: Fabri Fibra ft. Gianna Nannini - In Italia.
Queste settimane sono per me il periodo di apprendistato per la tesi, principalmente perché devo prendere confidenza con due cose: la meccanica statistica, della quale non so più di quanto abbia studiato per l'esame di Struttura della materia; e la programmazione, della quale, se non fosse stato per quel primo anno frequentato a Ingegneria, sarei completamente a digiuno.
Avevo già avuto modo di sfruttare il corso di Fondamenti di informatica nello scrivere le relazioni per il laboratorio di spettroscopia: i dati dell'ultimo esperimento (curva di Bragg) consistevano in 2800 file di testo; il professore ci aveva fornito due programmini per la loro analisi, ma sul mio pc non giravano, così rispolverai il manuale di Java e scrissi tutto ex novo. (Non era nulla di trascendentale: la parte più difficile fu imparare come far leggere al programma l'input da un file; il resto erano semplici operazioni sugli array.)
Ora però è Fortran (Fortran 90 per essere esatti) che devo imparare: per fortuna, essendo "roba vecchia" , non è stato troppo difficile trovare in biblioteca un manuale disponibile per il prestito.
Come benchmark, il relatore mi ha assegnato da simulare un fluido (argon) le cui particelle siano soggette a un potenziale di Lennard-Jones (forze di Van der Waals).
Potrei lavorare anche a casa, ma è meglio che stia in facoltà, visto che, se qualcosa non mi torna - evento assai frequente! - posso chiedere a un altro tesista, o al relatore stesso, o a un altro professore del gruppo - uno in particolare è da me ufficialmente adorato dopo che mi ha fatto capire i potenziali termodinamici (e le trasformazioni di Legendre) in meno di dieci minuti!
Ieri e oggi, dalla mia postazione - in una sorta di atrio, attrezzato con tre terminali - potevo sentire proprio uno di questi professori che interrogava degli studenti su fisica dello stato solido - l'esame che mi ha indirizzato verso questa tesi. L'andamento del calore specifico con la temperatura: i fononi, il modello di Debye, che si riduce alla legge di Dulong-Petit ad alte temperature... Non sono sadico, però che goduria avere finito e sapere che a stare sotto i riflettori ora tocca agli altri!
Canzone del giorno: Fabri Fibra ft. Gianna Nannini - In Italia.
lunedì 14 luglio 2008
Piazza Navona (1)
Otto anni fa, sentendo alla radio Sabbia bagnata, e ricordando Bambini, avessi avuto il blog avrei scritto: qualcuno salvi Paola Turci da Carmen Consoli.
Oggi, guardando i video del No Cav Day di martedì scorso a Piazza Navona, e ricordando la prima "stagione dei movimenti" , avendo il blog, scrivo: qualcuno salvi Marco Travaglio da Beppe Grillo.
Giusto per essere chiari: chi scrive non è un berlusconiano. E nemmeno un dalemiano, o un lettore del Riformista. Anzi, è uno che di libri di Marco Travaglio ne ha letti che metà basta. Che non si perdeva mai la rubrica Bananas sull'Unità. Che ancora adesso legge volentieri il suo blog - Voglio scendere, con Peter Gomez e Pino Corrias. Ma che disapprova l'atteggiamento che tiene da un paio d'anni a questa parte.
La sopra citata stagione dei girotondi - lanciata di prepotenza dallo storico intervento di Nanni Moretti ("Con questo tipo di dirigenti non vinceremo mai!"), proprio a Piazza Navona, il 2 febbraio 2002 - seguita dalle battaglie contro la censura in Rai, l'assalto al Corriere, le leggi vergogna, è stato indubbiamente un momento di grande vivacità. Con tanta partecipazione, l'affermazione di ideali di giustizia, di democrazia, di libertà d'informazione. Non senza un po' di tafazzismo, il quale tuttavia voleva essere una scrollata ad una sinistra evanescente.
Oggi lo scenario è completamente diverso. Mi fossi trovato a Roma martedì, non sarei sceso in piazza: sapevo che l'esito sarebbe stato quello che è stato.
Quelle persone che, qualche anno fa, ci facevano sentire di non essere soli, né loro mancava un certo ottimismo, ora sono incattivite. Chiuse in loro stesse, incapaci di comprendere la realtà - che è l'unica strada per affrontarla e tentare di cambiarla.
Oggi, guardando i video del No Cav Day di martedì scorso a Piazza Navona, e ricordando la prima "stagione dei movimenti" , avendo il blog, scrivo: qualcuno salvi Marco Travaglio da Beppe Grillo.
Giusto per essere chiari: chi scrive non è un berlusconiano. E nemmeno un dalemiano, o un lettore del Riformista. Anzi, è uno che di libri di Marco Travaglio ne ha letti che metà basta. Che non si perdeva mai la rubrica Bananas sull'Unità. Che ancora adesso legge volentieri il suo blog - Voglio scendere, con Peter Gomez e Pino Corrias. Ma che disapprova l'atteggiamento che tiene da un paio d'anni a questa parte.
La sopra citata stagione dei girotondi - lanciata di prepotenza dallo storico intervento di Nanni Moretti ("Con questo tipo di dirigenti non vinceremo mai!"), proprio a Piazza Navona, il 2 febbraio 2002 - seguita dalle battaglie contro la censura in Rai, l'assalto al Corriere, le leggi vergogna, è stato indubbiamente un momento di grande vivacità. Con tanta partecipazione, l'affermazione di ideali di giustizia, di democrazia, di libertà d'informazione. Non senza un po' di tafazzismo, il quale tuttavia voleva essere una scrollata ad una sinistra evanescente.
Oggi lo scenario è completamente diverso. Mi fossi trovato a Roma martedì, non sarei sceso in piazza: sapevo che l'esito sarebbe stato quello che è stato.
Quelle persone che, qualche anno fa, ci facevano sentire di non essere soli, né loro mancava un certo ottimismo, ora sono incattivite. Chiuse in loro stesse, incapaci di comprendere la realtà - che è l'unica strada per affrontarla e tentare di cambiarla.
domenica 13 luglio 2008
Entropia per principianti (1bis)
Ok, gente: dai vostri commenti mi rendo conto di non essermi affatto spiegato bene. Allora, ipotesi: forse non è chiaro il concetto di funzione di stato?
Be', vediamo prima cos'è uno stato.
Facciamo l'esempio che si fa a scuola: come sistema fisico prendiamo un gas in un recipiente.
Di quali informazioni ho bisogno per sapere tutto sullo stato del gas?
Innanzitutto c'è il volume del recipiente (V); poi la temperatura (T), la pressione (P) e il numero di particelle (N) che lo compongono.
Se il gas è ideale - cioè: le sue particelle sono assimilabili a microscopiche palle da biliardo - e all'equilibrio, queste quantità sono legate tra loro dalla nota equazione di stato PV = NkT, dove k è una costante (costante di Boltzmann).
Ebbene, queste quantità caratterizzano lo stato del gas. Ora, ho detto che l'entropia è una funzione di stato: che significa? Significa che, note queste quantità, è noto anche il valore dell'entropia.
Per dire: consideriamo l'aria che c'è nella stanza in cui vi trovate. Facciamo finta che le sue misure siano 4 x 5 x 2,7 m: un volume di 54 m3. Supponiamo anche che non faccia troppo caldo: una temperatura di 27 °C (Studio Aperto non si premuri di informarmi della temperatura percepita!); e di essere al livello del mare: una pressione di 1 atm. Ecco, sappiate che nella vostra stanza ci sono 1,32 · 1027 particelle, quadrilione più quadrilione meno.
Il gas nella vostra stanza ha il valore di entropia corrispondente.
Immaginiamo di prendere tutta quest'aria e di metterla in una bombola da 100 litri. Se la temperatura è la stessa, ora la pressione è 540 atm.
In questo nuovo stato, il gas ha un nuovo valore di entropia.
Ora, non ha importanza se io abbia aspirato tutta l'aria della stanza e l'abbia inserita nella bombola mantenendola a temperatura costante; oppure se l'abbia raffreddata sino a farla diventare liquida, l'abbia versata nella bombola e abbia atteso che la temperatura tornasse di 27 °C. Cioè non importa come è avvenuta la trasformazione: l'entropia del gas, dipendendo solo dallo stato, è cambiata della stessa quantità, e nel seguito vedremo come si trova questa variazione. (*)
Per la cronaca, in questo specifico caso la variazione vale -1,15 · 105 J/K. Cioè, l'entropia del sistema è diminuita.
E allora, cos'è questa storia che aumenta sempre?
Be', ora chiedete troppo.
Canzone del giorno: Angelo Branduardi - Cogli la prima mela.
(*) In effetti, ci interesseranno solo le variazioni di entropia, e non i suoi singoli valori.
Be', vediamo prima cos'è uno stato.
Facciamo l'esempio che si fa a scuola: come sistema fisico prendiamo un gas in un recipiente.
Di quali informazioni ho bisogno per sapere tutto sullo stato del gas?
Innanzitutto c'è il volume del recipiente (V); poi la temperatura (T), la pressione (P) e il numero di particelle (N) che lo compongono.
Se il gas è ideale - cioè: le sue particelle sono assimilabili a microscopiche palle da biliardo - e all'equilibrio, queste quantità sono legate tra loro dalla nota equazione di stato PV = NkT, dove k è una costante (costante di Boltzmann).
Ebbene, queste quantità caratterizzano lo stato del gas. Ora, ho detto che l'entropia è una funzione di stato: che significa? Significa che, note queste quantità, è noto anche il valore dell'entropia.
Per dire: consideriamo l'aria che c'è nella stanza in cui vi trovate. Facciamo finta che le sue misure siano 4 x 5 x 2,7 m: un volume di 54 m3. Supponiamo anche che non faccia troppo caldo: una temperatura di 27 °C (Studio Aperto non si premuri di informarmi della temperatura percepita!); e di essere al livello del mare: una pressione di 1 atm. Ecco, sappiate che nella vostra stanza ci sono 1,32 · 1027 particelle, quadrilione più quadrilione meno.
Il gas nella vostra stanza ha il valore di entropia corrispondente.
Immaginiamo di prendere tutta quest'aria e di metterla in una bombola da 100 litri. Se la temperatura è la stessa, ora la pressione è 540 atm.
In questo nuovo stato, il gas ha un nuovo valore di entropia.
Ora, non ha importanza se io abbia aspirato tutta l'aria della stanza e l'abbia inserita nella bombola mantenendola a temperatura costante; oppure se l'abbia raffreddata sino a farla diventare liquida, l'abbia versata nella bombola e abbia atteso che la temperatura tornasse di 27 °C. Cioè non importa come è avvenuta la trasformazione: l'entropia del gas, dipendendo solo dallo stato, è cambiata della stessa quantità, e nel seguito vedremo come si trova questa variazione. (*)
Per la cronaca, in questo specifico caso la variazione vale -1,15 · 105 J/K. Cioè, l'entropia del sistema è diminuita.
E allora, cos'è questa storia che aumenta sempre?
Be', ora chiedete troppo.
Canzone del giorno: Angelo Branduardi - Cogli la prima mela.
(*) In effetti, ci interesseranno solo le variazioni di entropia, e non i suoi singoli valori.
venerdì 11 luglio 2008
Entropia per principianti (1)
1. La seconda legge della termodinamica e le macchine termiche
Come avevo anticipato, l'ingrediente fondamentale per parlare di entropia è la seconda legge della termodinamica - la prima non è altro che la conservazione dell'energia.
Ce ne sono due celebri - equivalenti - formulazioni:
Supponiamo che la "macchina proibita di Kelvin" sia installata su una nave. La nave assorbirebbe calore dal mare, lo trasformerebbe per intero in lavoro motore e, con l'attrito tra scafo ed acqua, compenserebbe la perdita di calore del mare.
La fonte di calore sarebbe una sola (il mare), la conservazione dell'energia sarebbe rispettata: un perfetto moto perpetuo. Ma le compagnie petrolifere dormano sonni tranquilli: è fisicamente impossibile.
Una macchina termica opera tra (almeno) due sorgenti - nel seguito, T1 e T2 indicheranno sia le temperature delle sorgenti che le sorgenti stesse - T2 (calda) da cui preleva il calore Q2; T1 (fredda) a cui cede il calore Q1 non trasformato in lavoro.
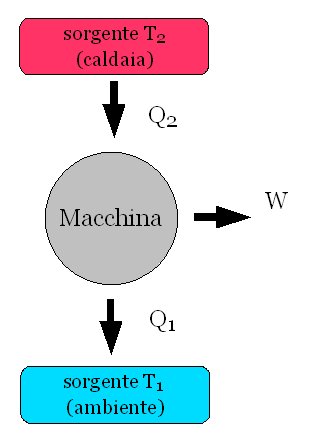
Entrambe le sorgenti, schematicamente, sono considerate termostati: apparati talmente grandi da poter cedere o assorbire calore senza variazione di temperatura.
Il bilancio energetico della macchina si esprime perciò nella relazione Q2 - W - Q1 = 0 (essendo il funzionamento ciclico, il "dare/avere" energetico deve risultare pari). La quantità η = W/Q2 = 1 - Q1/Q2 si chiama rendimento della macchina (lavoro utile sviluppato / costo energetico): l'enunciato di Kelvin mi garantisce che è sempre η < 1.
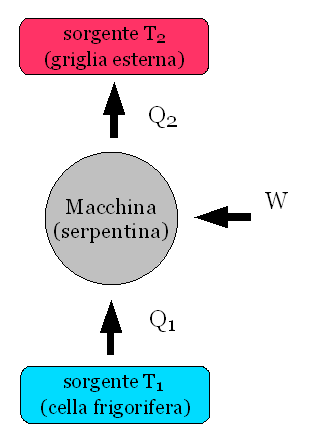
In quest'altra figura è schematizzato un frigorifero: stavolta il bilancio si scrive W - Q2 + Q1 = 0. Il lavoro è compiuto da un motore esterno (il motore del frigorifero) e serve per "pompare" calore dalla cella all'esterno (griglia): senza di esso, niente gelati!
Niente di così complicato per ora, vero? Sperando di non essere stato troppo serioso, vi do l'arrivederci per la seconda puntata ;-)
Come avevo anticipato, l'ingrediente fondamentale per parlare di entropia è la seconda legge della termodinamica - la prima non è altro che la conservazione dell'energia.
Ce ne sono due celebri - equivalenti - formulazioni:
- enunciato di Kelvin-Planck: è impossibile trasformare completamente in lavoro il calore prelevato da una sorgente a temperatura uniforme;
- enunciato di Clausius: è impossibile che, senza lavoro esterno, si trasferisca calore da un corpo ad un altro a temperatura maggiore.
Supponiamo che la "macchina proibita di Kelvin" sia installata su una nave. La nave assorbirebbe calore dal mare, lo trasformerebbe per intero in lavoro motore e, con l'attrito tra scafo ed acqua, compenserebbe la perdita di calore del mare.
La fonte di calore sarebbe una sola (il mare), la conservazione dell'energia sarebbe rispettata: un perfetto moto perpetuo. Ma le compagnie petrolifere dormano sonni tranquilli: è fisicamente impossibile.
Una macchina termica opera tra (almeno) due sorgenti - nel seguito, T1 e T2 indicheranno sia le temperature delle sorgenti che le sorgenti stesse - T2 (calda) da cui preleva il calore Q2; T1 (fredda) a cui cede il calore Q1 non trasformato in lavoro.

Entrambe le sorgenti, schematicamente, sono considerate termostati: apparati talmente grandi da poter cedere o assorbire calore senza variazione di temperatura.
Il bilancio energetico della macchina si esprime perciò nella relazione Q2 - W - Q1 = 0 (essendo il funzionamento ciclico, il "dare/avere" energetico deve risultare pari). La quantità η = W/Q2 = 1 - Q1/Q2 si chiama rendimento della macchina (lavoro utile sviluppato / costo energetico): l'enunciato di Kelvin mi garantisce che è sempre η < 1.

In quest'altra figura è schematizzato un frigorifero: stavolta il bilancio si scrive W - Q2 + Q1 = 0. Il lavoro è compiuto da un motore esterno (il motore del frigorifero) e serve per "pompare" calore dalla cella all'esterno (griglia): senza di esso, niente gelati!
Niente di così complicato per ora, vero? Sperando di non essere stato troppo serioso, vi do l'arrivederci per la seconda puntata ;-)
sabato 5 luglio 2008
Entropia per principianti (intro)
Con il suo trattatello semiserio sull'entropia, Marina di inezie essenziali ha imprudentemente svegliato il cane dormiente ;-)
Entropia: una parola usata e strausata, ma cosa realmente sia pochi sanno.
A scuola, nell'ora di biologia o di chimica, ci dicono che è una misura della dissipazione di energia o del disordine di un sistema fisico.
Quest'ultima definizione, a mio modo di vedere, è totalmente fuorviante - come dice la mia ragazza: io trovo più ordinato un impasto omogeneo di uova e farina che le uova e la farina separate! - la prima già è più precisa; ma quando si parla di una grandezza fisica è sempre meglio definirla esattamente, lasciando a dopo le implicazioni, in particolare quelle più suggestive - come la macabra morte termica.
È vero che l'entropia è l'ultimo argomento della termodinamica classica, tema che rientra ampiamente nei programmi scolastici di fisica; spesso tuttavia non si riesce a trattarlo con la dovuta cura, tenuto conto anche della notevole astrazione necessaria alla sua comprensione - già nel concetto di trasformazione reversibile.
Ora, è vero che il titolo di questo e dei successivi post è Entropia per principianti, ma non spaventatevi alla prospettiva di spiegazioni rigorose: la fisica non è una disciplina per geni, basta che non pretendiamo di capire tutto e subito, e che abbiamo un po' di fiducia in noi stessi.
Cominciamo col dire che l'entropia non è una cosa cattiva: è una funzione di stato - vedremo com'è costruita - di un sistema fisico. In altre parole, è una grandezza che dipende dai suoi parametri (pressione, temperatura, numero di particelle...): la variazione di entropia, a seguito di una trasformazione, non dipende da come la trasformazione è avvenuta, ma solo dagli stati iniziale e finale.
Ci si chiede: ma se il sistema compie una trasformazione ciclica - cioè, torna allo stato iniziale; è quello che accade in una macchina - com'è che l'entropia aumenta? Perché a scuola ci dicono che aumenta sempre!
In effetti non aumenta sempre l'entropia del sistema, ma quella dell'universo (sistema + ambiente esterno); è l'entropia di un sistema isolato - che non scambia materia né energia con l'esterno - ad avere la caratteristica di aumentare qualunque trasformazione abbia luogo. Un sistema che scambia energia con l'ambiente (per dire: un recipiente con pareti conduttrici) non è isolato, ma l'insieme sistema + ambiente (universo termodinamico) è da considerarsi isolato.
Come costruiremo la funzione di stato entropia?
Canzone del giorno: Kim Lukas - To Be You.
Entropia: una parola usata e strausata, ma cosa realmente sia pochi sanno.
A scuola, nell'ora di biologia o di chimica, ci dicono che è una misura della dissipazione di energia o del disordine di un sistema fisico.
Quest'ultima definizione, a mio modo di vedere, è totalmente fuorviante - come dice la mia ragazza: io trovo più ordinato un impasto omogeneo di uova e farina che le uova e la farina separate! - la prima già è più precisa; ma quando si parla di una grandezza fisica è sempre meglio definirla esattamente, lasciando a dopo le implicazioni, in particolare quelle più suggestive - come la macabra morte termica.
È vero che l'entropia è l'ultimo argomento della termodinamica classica, tema che rientra ampiamente nei programmi scolastici di fisica; spesso tuttavia non si riesce a trattarlo con la dovuta cura, tenuto conto anche della notevole astrazione necessaria alla sua comprensione - già nel concetto di trasformazione reversibile.
Ora, è vero che il titolo di questo e dei successivi post è Entropia per principianti, ma non spaventatevi alla prospettiva di spiegazioni rigorose: la fisica non è una disciplina per geni, basta che non pretendiamo di capire tutto e subito, e che abbiamo un po' di fiducia in noi stessi.
Cominciamo col dire che l'entropia non è una cosa cattiva: è una funzione di stato - vedremo com'è costruita - di un sistema fisico. In altre parole, è una grandezza che dipende dai suoi parametri (pressione, temperatura, numero di particelle...): la variazione di entropia, a seguito di una trasformazione, non dipende da come la trasformazione è avvenuta, ma solo dagli stati iniziale e finale.
Ci si chiede: ma se il sistema compie una trasformazione ciclica - cioè, torna allo stato iniziale; è quello che accade in una macchina - com'è che l'entropia aumenta? Perché a scuola ci dicono che aumenta sempre!
In effetti non aumenta sempre l'entropia del sistema, ma quella dell'universo (sistema + ambiente esterno); è l'entropia di un sistema isolato - che non scambia materia né energia con l'esterno - ad avere la caratteristica di aumentare qualunque trasformazione abbia luogo. Un sistema che scambia energia con l'ambiente (per dire: un recipiente con pareti conduttrici) non è isolato, ma l'insieme sistema + ambiente (universo termodinamico) è da considerarsi isolato.
Come costruiremo la funzione di stato entropia?
- L'ingrediente fondamentale è la seconda legge della termodinamica. Probabilmente la conoscete già, ma la formuleremo rigorosamente;
- poi ci servono due teoremi: il teorema di Carnot e il teorema di Clausius - a quest'ultimo scienziato si deve il termine entropia, che vuol dire trasformazione. Li dimostreremo entrambi - abbiate pazienza, ma fare scienza senza dimostrazioni è come tradurre un testo con un traduttore automatico;
- a questo punto avremo tutte le informazioni per dare la definizione di entropia. Vedremo, in particolare, perché l'entropia di un sistema isolato aumenta sempre, restando costante nel solo caso limite - e irrealistico - di trasformazioni reversibili;
- vedremo alcuni esempi, chiarendo il concetto approssimativo di variazione di entropia come misura dell'irreversibilità della trasformazione, o dell'energia sprecata, cioè non più trasformabile in lavoro utile.
Canzone del giorno: Kim Lukas - To Be You.
giovedì 3 luglio 2008
Arcus non caelestis
My heart leaps up when I behold
A rainbow in the sky:
So was it when my life began;
So is it now I am a man;
So be it when I shall grow old,
Or let me die!
The Child is father of the Man;
I could wish my days to be
Bound each to each by natural piety.
(William Wordsworth, 1802)
A rainbow in the sky:
So was it when my life began;
So is it now I am a man;
So be it when I shall grow old,
Or let me die!
The Child is father of the Man;
I could wish my days to be
Bound each to each by natural piety.
(William Wordsworth, 1802)
 Fu un sacerdote - padre Alex Zanotelli - a lanciare, nel 2002, l'iniziativa Pace da tutti i balconi, come protesta contro la (allora ipotetica) guerra in Iraq. In pochissimo tempo i condomini delle nostre città si popolarono dello stendardo arcobaleno con la scritta pace.
Fu un sacerdote - padre Alex Zanotelli - a lanciare, nel 2002, l'iniziativa Pace da tutti i balconi, come protesta contro la (allora ipotetica) guerra in Iraq. In pochissimo tempo i condomini delle nostre città si popolarono dello stendardo arcobaleno con la scritta pace.La partecipazione coinvolse, tra gli altri, numerosi uomini di Chiesa, religiosi e laici; ma quando il simbolo iridato cominciò ad essere strumentalizzato dai partiti di sinistra - il quotidiano l'Unità lo mise accanto al titolo - lo stesso Zanotelli fu tra i firmatari di una lettera aperta in cui, tra le altre cose, si afferma che il valore politico di questo movimento non può e non deve essere ingabbiato all'interno di partiti e schieramenti elettorali.
Nel frattempo, dagli ambienti ecclesiastici si levò più di una voce contraria a quei sacerdoti che usavano la bandiera arcobaleno al posto della tovaglia bianca sull'altare. Il comunicato del 20 giugno scorso dell'agenzia vaticana Fides, dal titolo L'arcobaleno: sincretismo o pace?, ne è l'ultimo atto.
Ora, al di là della scarsa attualità dell'argomento - i balconi d'Italia sono ormai vuoti, e le bandiere rimaste sono annerite dallo smog - è giusto ribadire che la Messa è un momento di preghiera, non un raduno hippie o un comizio politico (di alcuna parte!); che quindi, al centro, debba esserci Gesù. Il simbolo principale della pace, nel Cristianesimo, è la croce di Cristo morto per amore; ed è il Suo amore, il Suo sacrificio che noi dobbiamo sempre avere in mente, non i crimini commessi in Suo nome.
Anche questo è scritto nel comunicato di Fides. Ma, allora, se non è il simbolo della croce in sé stesso ad aver bisogno di essere emendato quanto piuttosto gli atteggiamenti degli uomini, perché la cosa non vale anche per l'arcobaleno, che nella Bibbia è il simbolo dell'alleanza tra Dio e il creato, dopo il diluvio?

«Il mio arco pongo sulle nubiIl sito mariadinazareth giustifica la correlazione tra bandiera arcobaleno e movimenti teosofici-new age - nel testo di Fides, in realtà, non è dimostrato alcun legame diretto - con la disposizione dei colori nella bandiera della pace, rovesciata rispetto a come normalmente si osserva l'arco in cielo: un messaggio subliminale di lotta contro la legge di Dio.
ed esso sarà il segno dell'alleanza
tra me e la terra.
Quando radunerò
le nubi sulla terra
e apparirà l'arco sulle nubi
ricorderò la mia alleanza
che è tra me e voi
e tra ogni essere che vive in ogni carne
e non ci saranno più le acque
per il diluvio, per distruggere ogni carne.» (Genesi 9, 14-15)
 Senza voler fare della scontata ironia, questa è una forzatura. Primo, per una ragione scientifica: accade di rado, ma non così tanto, che esternamente all'arco principale si noti l'arco secondario, dallo spettro invertito. (E, ancora più di rado, archi di ordine superiore.) Un fenomeno, ironia della sorte, spiegato per la prima volta da un domenicano, Dietrich von Freiberg. Secondo, perché se così stanno le cose, gli omosessuali sono tutto tranne che contro natura, dal momento che la loro bandiera arcobaleno ha la disposizione corretta.
Senza voler fare della scontata ironia, questa è una forzatura. Primo, per una ragione scientifica: accade di rado, ma non così tanto, che esternamente all'arco principale si noti l'arco secondario, dallo spettro invertito. (E, ancora più di rado, archi di ordine superiore.) Un fenomeno, ironia della sorte, spiegato per la prima volta da un domenicano, Dietrich von Freiberg. Secondo, perché se così stanno le cose, gli omosessuali sono tutto tranne che contro natura, dal momento che la loro bandiera arcobaleno ha la disposizione corretta.Approfitto per rispondere a una domanda che lo stesso sito si pone in un'altra pagina: perché i colori dell'iride sono proprio sette? Questione mal posta: i colori sono infiniti, come infinite - percezione umana e principio di indeterminazione tempo-energia permettendo - sono le lunghezze d'onda fra 380 e 750 nm. La sequenza che si impara alla scuola elementare - rosso, arancio, giallo, verde, azzurro, indaco, violetto - è dovuta a Newton, che originariamente contava solo cinque colori; arancio e indaco furono aggiunti, sempre da lui, per analogia con la scala musicale.
Canzone del giorno: The Fratellis - Henrietta.
Iscriviti a:
Commenti (Atom)