Essendo trascorso quasi un mese dall'ultima semi-puntata, facciamo il punto di quanto finora abbiamo visto:
- secondo principio della termodinamica (enunciato di Clausius): non si può trasferire spontaneamente calore da un corpo ad un altro a temperatura maggiore;
- secondo principio della termodinamica (enunciato di Kelvin-Planck): una macchina termica non può trasformare interamente in lavoro il calore Q2 prelevato dalla caldaia T2; ne cederà sempre una parte Q1 a una sorgente a temperatura inferiore T1 (tipicamente, l'ambiente esterno);
- rendimento di una macchina termica: è il rapporto tra il lavoro utile sviluppato W = Q2 - Q1 e il calore assorbito Q2. In parole povere, è il rapporto beneficio/costo: per l'enunciato di Kelvin, è sempre minore di 1;
- trasformazioni reversibili: sono quelle che, con una minima variazione delle condizioni esterne, possono essere invertite senza modificare l'ambiente. Sono un caso limite: per essere considerata reversibile, una trasformazione deve avvenire in un tempo estremamente lungo e in assenza di forze dissipative.
Date due sorgenti di calore T1 < T2, tutte le macchine reversibili che operano tra esse, comunque siano costruite, hanno lo stesso rendimento; e qualsiasi macchina irreversibile operante tra esse ha rendimento inferiore.
Una macchina di Carnot è una macchina reversibile che lavora tra due sorgenti. Per conoscerne il rendimento, essendo uguale per tutte, lo si può calcolare in un caso semplice, come quello di una macchina a gas ideale.
Il ciclo di Carnot a gas ideale è composto di quattro trasformazioni, ovviamente tutte reversibili:
- espansione isoterma: le pareti del recipiente (cilindro del motore) conducono calore, ed esso è a contatto con la sorgente calda T2. Espandendosi, il gas tenderebbe a raffreddarsi, per cui assorbe calore da T2 per mantenersi a detta temperatura;
- espansione adiabatica: ora le pareti sono isolanti (adiabatica è una trasformazione dove non si scambia calore con l'esterno), e il gas si raffredda. Lo si fa raffreddare fino alla temperatura T1 della sorgente fredda;
- compressione isoterma: le pareti sono di nuovo conduttrici, il cilindro è a contatto con la sorgente T1, alla quale cede calore poiché, comprimendosi, il gas tenderebbe a riscaldarsi;
- compressione adiabatica: le pareti sono di nuovo isolanti, e si riporta il gas alla temperatura T2, per poi ripetere il ciclo.
Queste trasformazioni corrispondono rispettivamente alle fasi di espansione, scarico, aspirazione, compressione di un motore Diesel. La corrispondenza è peraltro piuttosto vaga poiché nel ciclo di Carnot niente viene aspirato o scaricato: le pareti del cilindro sono sempre chiuse.
Ora, sfruttando le proprietà del gas ideale, si potrebbe dimostrare (non lo facciamo) che il rendimento della macchina di Carnot vale:
Le temperature sono espresse in kelvin. Si vede subito che questo numero è compreso tra 0 e 1, rispettando così i principi della termodinamica. L'unico modo per avere η = 1 sarebbe T1 = 0, cioè la sorgente fredda allo zero assoluto, temperatura fisicamente non raggiungibile.
Il punto cruciale però è: perché non si può avere, con le stesse sorgenti, un rendimento maggiore?
Ecco il perché:
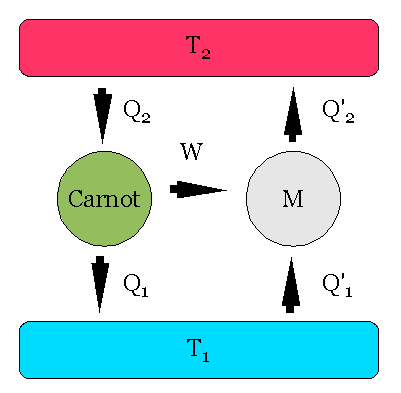
Una macchina di Carnot è usata per alimentare la macchina M, che lavora come frigorifero.
Considerando le due macchine come un unico apparato, deve essere Q2 ≤ Q'2, perché altrimenti avrei un trasferimento netto di calore da T1 a T2, più caldo, contro l'enunciato di Clausius.
Il bilancio energetico delle due macchine mi dà Q2 - Q1 = Q'2 - Q'1 = W; così
ed essendo Q2/Q'2 ≤ 1, è dimostrato che il rendimento di M non può superare quello della macchina di Carnot.
Se anche M è reversibile, si può invertire tutto il processo, ottenendo la diseguaglianza inversa; di conseguenza i due rendimenti sono uguali.
Canzone del giorno: Modjo - No More Tears.
me lo ricordo Carnot :)
RispondiEliminabella la canzone di Modjo
ciao, io non me lo ricordo e visto che me l'hai chiesto te lo dico, mica l'ho letto sto post. Però, e dico però, ammetto che è per ignoranza mia, mica perchè sia inutile o scritto male, ok???
RispondiEliminamagari un altro giorno che sono meno in coma ci provo, ok?
mav